„In der Forschung tut sich wahnsinnig viel“, sagt Professor Hermann Reichenspurner. „Rund um den Globus sind Wissenschaftler in ihren Laboren damit beschäftigt, nach Möglichkeiten zu suchen, um die Lebensqualität von Menschen zu verbessern und ihr Leben zu verlängern. Selbstverständlich wird auch bei uns im UKE mit größter Präzision, Akribie und unendlicher Geduld gearbeitet. Ich habe größten Respekt vor den Menschen, die oft jahrelang damit beschäftigt sind, um eine Lösung, eine Verbesserung, zu finden.“
WORUM GEHT ES DEN WISSENSCHAFTLERN?
Zum Beispiel darum, herauszufinden, warum Arterienverengungen überhaupt entstehen. Oder um das Ziel, ein vollimplantierbares Kunstherz als Alternative zur Herztransplantation zu entwickeln. Denn täglich sterben weltweit Menschen auf der Warteliste, weil kein lebensrettendes Spenderorgan zur Verfügung steht. Und die Spendebereitschaft hat sich aufgrund der Manipulation von Empfängerlisten nicht gerade verbessert.
Die Herzchirurgie kann derzeit sogenannte teilimplantierbare Kunstherzen nutzen. Teilimplantierbar bedeutet jedoch für den betroffenen Patienten, dass bei diesen mechanischen Geräten Druckschläuche aus der Bauchdecke ragen. Um ein hohes Maß an Lebensqualität zu gewährleisten, wird in Deutschland das Kunstherz ReinHeart als vollimplantierbares System entwickelt – ohne Schläuche oder Kabel, die die Haut des Patienten durchstoßen. Obendrein muss das System völlig wartungsfrei über viele Jahre im Körper des Menschen schlagen, was extrem hohe Anforderungen an den Entwicklungsprozess stellt: Die ausreichende Funktionssicherheit und Langlebigkeit bei gleichzeitiger Miniaturisierung des Systems müssen gewährleistet sein. Um all diese Anforderungen zu realisieren, arbeiten Ingenieure, Techniker und Ärzte bei der Entwicklung eng zusammen.
STAMMZELLEN REPARIEREN KRANKE HERZMUSKEL
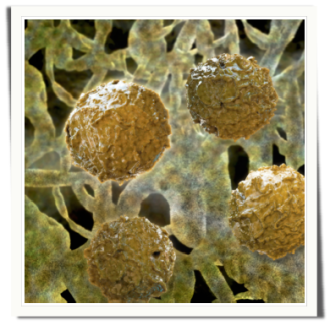
Bis zu einer Milliarde Muskelzellen sterben bei einem Herzinfarkt ab. Um sowohl den Schaden am Herzen zu begrenzen, als auch den kranken Muskel zu regenerieren, setzen Wissenschaftler in aller Welt auf Stammzellen. Aus diesen Vorläuferzellen lassen sich nicht nur sämtliche das menschliche Herz bildende Zelltypen generieren, sondern auch bereits funktionelles Herzgewebe gewinnen.
„Noch ist allerdings unklar, welche Art von Stammzellen den größten Nutzen bringen wird“, sagt Prof. Sonja Schrepfer, eine von der Deutschen Forschungsgemeinschaft mit einer Heisenberg-Professur ausgezeichnete Wissenschaftlerin.
Sie leitet die Forschergruppe TSI (Transplant and Stem Cell Immunobiology Lab) am UKE.Das Ziel ihrer Forschung: Kranke Herzmuskeln mit Stammzellen zu reparieren. Adulte, also erwachsene Stammzellen aus dem Knochenmark, können beim akuten Infarkt Herzmuskelzellen oft vor einem Sauerstoffmangel schützen und somit das Infarktausmaß eindämmen. Auch Zellen aus dem Nabelschnurblut werden gewisse regenerative Fähigkeiten zugeschrieben.
Liegt der Infarkt jedoch länger zurück und das abgestorbene Gewebe ist bereits vernarbt, können sogenannte induzierte pluripotente Stammzellen ( iPS-Zellen) hilfreich sein: iPS-Zellen können sich, ähnlich wie embryonale Stammzellen, zu jedem Zelltyp entwickeln und sind noch auf keinen Gewebetyp festgelegt. Um iPS-Zellen zu gewinnen, ist lediglich eine kleine Hautprobe erforderlich. „Daraus werden Zellen isoliert, die dann zu Stammzellen umprogrammiert werden können, aus denen sich anschließend Herzmuskelzellen entwickeln sollen“, erläutert die Wissenschaftlerin den komplexen Mechanismus. Die Rückentwicklung von Haut- in Stammzellen erfolgt mithilfe von manipulierten Viren, die mit genetischen Informationen beladen sind und diese in die Zellen einschleusen.
ABSTOSSUNGS-REAKTIONEN VERHINDERN
Ein weiteres Forschungsschwerpunkt ist die Suche nach Möglichkeiten, das Immunsystem zu überlisten, so dass es gewebefremde, transplantierte Stammzellen nicht als fremd erkennt und attackiert. Gingen
die Forscher bis vor wenigen Jahren davon aus, dass Stammzellen aufgrund ihres frühen Entwicklungsstadiums keine Immunreaktion im Empfänger auslösen, wissen sie heute, dass bestimmte
Oberflächenmoleküle auch bei Stammzellen einen Abstoßungsprozeß in Gang setzen. „Wir können Herzpatienten natürlich nicht lebenslang mit Medikamenten, die das Immunsystem unterdrücken, versorgen.
Dies würde zu schweren Nebenwirkungen wie Nierenversagen oder Diabetes bei den ohnehin schwer kranken Menschen führen“, erläutert Prof. Schrepfer. „Also müssen wir Möglichkeiten finden, die den
Patienten nicht noch zusätzlich belasten.“
HERZINFARKTE FRÜHESTMÖGLICH ERKENNEN
Eine weitere UKE-Arbeitsgruppe beschäftigt sich mit neuen Tests zur Früherkennung des Herzinfarktes. Ziel ist es, Eiweiße im Blut zu isolieren, die einen drohenden Herzinfarkt anzeigen und dem Arzt eine Behandlung noch vor Untergang von Herzmuskelgewebe ermöglichen.
Eine andere Arbeitsgruppe untersucht die Bedeutung weisser Blutkörperchen (Leukozyten) und deren Enzymsysteme für die Entstehung von Herzkranzgefäßerkrankungen und Herzschwäche. Projekte, die zum Teil durch den Förderverein des Herzzentrums unterstützt werden, untersuchen die Bedeutung dieser Enzyme für die Regulation des Gefäßtonus und des strukturellen Umbaus des Herzmuskels. Diese Arbeitsgruppe war die erste, die den Einfluss des Enzyms auf die Gefäßerweiterung beschrieben hat und die weltweit erste, die zeigen konnte, dass erhöhte Spiegel des Enzyms im Blut das Risiko für das Entstehen eines Herzinfarktes bei Patienten mit Brustschmerz anzeigen.
OHNE OPERATION AM OFFENEN HERZEN
Die kathetergestützte Behandlung von Herzklappenfehlern, insbesondere bei Verengung der Auslassklappe (Aortenstenose) und Undichtigkeit der Einlassklappe (Mitralklappeninsuffizienz) stellt einen weiteren zentralen Forschungsschwerpunkt im Herzzentrum am UKE dar.
In der Klinik für Kardiologie mit Schwerpunkt Elektrophysiologie sind gleich mehrere Forschungsbereiche etabliert. Diese beinhalten Arbeiten zur Optimierung des Verständnisses und der Therapie von
anfallsartigen (paroxysmalen) und durchgehenden (persistierenden) Vorhofflimmern.
Weitere Forschungsschwerpunkte sind:
- Reparatur von Herzklappen
- Katheterbasierter Aortenklappenersatz
- Organkonservierung für Transplantationen
- Entwicklung neuer minimal-invasiver und endoskopischer Operationsverfahren mit Robotik
- Entwicklung neuer Systeme für die Herz-Lungen-Maschine
- Vergleich von biologischen Herzklappen
- Endothelforschung
- Einsatz von neuen biventrikulären Herzschrittmachersystemen
- Experimentelle Herz- und Lungentransplantation
- Experimenteller und klinischer Einsatz neuer immunsuppressiver Substanzen, die Abstoßungsreaktionen des Körpers auf schonendere Weise verhindern sollen.